边缘区淋巴瘤的规范诊治++第四届中国淋巴瘤个体化治疗大会
- 分类:其他血液病
- 作者:编辑
- 来源:互联网
- 发布时间:2021-03-25 14:33
- 访问量:
【概要描述】MZL概述:流行病学及相关危险因素 边缘区淋巴瘤(MZL)是一组起源于淋巴滤泡的边缘区B细胞淋巴瘤,可发生于脾、淋巴结和黏膜淋巴组织,约占所有非霍奇金淋巴瘤(NHL)的10%。MZL的发病率较低,在西方国家发病率约为5%-15%,在中国的发病率为7.8%。MZL存在较强的异质性,WHO将MZL分为三种类型:结外粘膜相关淋巴组织(MALT)淋巴瘤(EMZL)、脾边缘区B细胞淋巴瘤(SMZL)、淋巴结边缘区淋巴瘤(NMZL),其中MALT淋巴瘤最为常见,约占70%。MZL呈惰性,预后相对较好。EMZL的中位总生存期(OS)>12年,SMZL和NMZL的中位OS>8年。 目前普遍认为MALT淋巴瘤的发生可能与慢性抗原刺激有关,如感染或自身免疫性疾病。幽门螺杆菌、空肠弯曲菌分别与胃、肠MALT淋巴瘤有比较确切的关系。眼附属器MALT淋巴瘤与鹦鹉热衣原体感染相关,皮肤MALT淋巴瘤与疏螺旋体感染存在相关性,HCV感染可致多部位MALT淋巴瘤发生,如脾、唾液腺或泪腺。目前尚未确定肺MALT淋巴瘤的致病原,吸烟与发病关系存在争议。约15%的原发肺MALT淋巴瘤患者合并有自身免疫病,包括多发性硬化、系统性红斑狼疮(SLE)、桥本甲状腺炎、干燥综合征,均为肺MALT淋巴瘤发生的危险因素。 MZL的诊治规范 MZL的病理特征包括肿瘤中包含大量异质性细胞浸润,有中心样细胞、单核细胞、B细胞、小淋巴细胞和浆细胞等,也可能有大细胞和/或幼稚细胞存在。患者生存时间大多数较长,但也有少数病例可呈侵袭性疾病进程。MZL肿瘤细胞表达B细胞相关抗原,如CD19、CD20、CD22、CD79b,MZL患者通常CD10-、CD5-、CD43±、CD3-、CD23-、CD11c±,少数结外患者可见CD5+。MZL亚型的生物机制各不相同,主要通路为NF-κB和NOTCH通路。 对于MZL的病理诊断,双跃荣教授强调了克隆性IG基因重排检测的重要性。部分MALT淋巴瘤可出现t(11;18),预示疾病晚期和抗HP治疗疗效欠佳,需要采用其他治疗方式。对于SMZL,可检测-7q+,3q等染色体异常或NOTCH2、KLF2等基因突变。SMZL可通过检测MYD88突变和淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)鉴别,以及检测BRAF突变与毛细胞白血病进行鉴别。 非胃MALT或NMZL适用Lugano分期,而胃肠MZL则采用AnnArbor分期系统的Lugano改良版或胃肠淋巴瘤的TNM分期(巴黎分期)。SMZL通常为脾单发,通过脾切除进行诊断和分期。 MALT淋巴瘤、SMZL、NMZL拥有各自独立的预后评估系统,相关基因异常可提示预后。MALT淋巴瘤采用IELSG预后模型(MALT-IPI),通过年龄、分期、乳酸脱氢酶(LDH)等危险因素对MALT淋巴瘤患者进行分层。一项基于人群的研究显示:EMZL原发部位和诊断时期对患者的死亡率存在影响。原发部位为泌尿生殖(GU)系统的EMZL患者预后最差,而位于皮肤和结缔组织的患者预后最好。C-myc过表达同样可以预测MALT淋巴瘤的预后不良。一项对62例MALT淋巴瘤患者进行的多因素分析显示,C-myc≥20%具有显著统计学差异。 滤泡性淋巴瘤(FL)的预后指标24月内疾病进展(POD24)在MALT淋巴瘤中同样提示预后不良。IELSG19临床研究显示:接受一线系统性治疗的EMZL患者,出现POD24患者生存率较差,有可能作为未来前瞻性临床研究的终点指标。MALT淋巴瘤出现组织学转化同样提示预后不良。微小残留病(MRD)评估是SMZL的独立预后因素。相关研究显示:骨髓中uMRD(定义为MRD<0.01%)是SMZL患者,尤其是治疗结束后达到部分缓解(PR)的患者的独立预后因素。 双跃荣教授随后对MZL的治疗方式进行了介绍。对于早期病灶局限的MZL患者,治疗以局部治疗为主,包括手术和局部放疗等。对于一线治疗无效局限期患者或晚期全身广泛受累的MZL患者,由于其惰性病程,治疗参考FL,有治疗指征的患者采用系统性免疫化疗。对于复发难治MZL患者可选择来那度胺、BTK抑制剂、PI3K抑制剂、嵌合抗原受体T细胞(CAR-T)等新药治疗。 抗HP治疗是早期胃MALT淋巴瘤的首选治疗方式,相关研究显示:单纯HP治疗可带来长期缓解,完全缓解(CR)率达到80%,71%的患者可获得持续5年的CR,5年总生存(OS)率达到90%。但对于t(11;18)阳性患者,抗HP治疗CR率仅为15%,t(11;18)阳性与治疗无反应及复发显著相关,对于这部分患者需要选择其他治疗方式。局部胃MALT淋巴瘤放射治疗的10年长期随访结果显示:所有患者接受放射治疗后内镜活检均获得CR,5年和10年OS率分别为92%和87%,5年和10年无复发生存(RFS)率分别为88%和77%。目前NCCN指南也推荐放射治疗作为HP阴性和抗生素治疗无效MZL患者的治疗选择。 目前各指南中MALT淋巴瘤的一线治疗方案大多为利妥昔单抗为基础联合放化疗,根据疾病分期和分型选择合适的一线治疗方案。 Stil NHL 7-2008研究探索了BR方案(苯达莫司汀+利妥昔单抗)治疗MZL后利妥昔单抗维持治疗的必要性。研究结果显示:BR治疗后2年利妥昔单抗维持治疗延长了患者的PFS(HR:0.33),但OS无差异。BR方案治疗后利妥昔单抗的维持治疗对于MZL患者是一种可行的治疗方法。 MZL的最新治疗进展 MZL存在众多潜在的治疗靶点,无论是针对MZL一线治疗的R2方案(来那度胺+利妥昔单抗)还是针对复发难治MZL的PI3K/AKT/mTOR抑制剂、BTK抑制剂、CAR-T疗法都值得进行探索。 2020年ASH大会上报道的一项多中心队列研究探索了伊布替尼治疗复发难治MZL的预测因素和结果,研究结果显示:伊布替尼治疗线数不同,PFS或OS无显著差异(2 vs 3 vs 4线及以后);伊布替尼治疗达到CR/PR以及没有复杂细胞遗传学是更好的PFS和OS预测指标。PCYC-1121研究纳入了63例复发难治MZL患者接受伊布替尼治疗。中位随访33.1个月时,伊布替尼治疗复发难治MZL的客观缓解率(ORR)达到58%,缓解持续时间(DOR)为27.6个月,中位PFS为15.7个月,中位OS未达到;在随后14个月中未出现新的不良事件(AE)。该研究同时显示:2项基因突变(A20和MYD88L265P)与预后较好(SPD、PFS)相关;2项基因突变(KMT2D和CARD11)与预后较差(DOR)相关。 2020年ASH大会上同样公布了PI3K抑制剂Parascalisib治疗复发难治MZL的疗效和安全性(CITADEL研究)。研究结果显示:Parascalisib治疗复发难治MZL的ORR达到57%,中位DOR和PFS分别为12个月和19.4个月。 ZUMA-5研究探索了靶向CD19的CAR-T产品axicabtagene ciloleucel(axi-cel)治疗NHL的疗效,研究共纳入22例MZL患者。ZUMA-5研究结果显示:axi-cel治疗MZL的ORR达到85%,CR率为60%,中位DOR为10.6个月;MZL组患者的中位PFS为11.8个月,12个月PFS率为45.1%,中位OS未达到,12个月OS率为92.9%。 总结 双跃荣教授最后总结道:MZL是来源于B细胞的惰性淋巴瘤,其病因与多种微生物慢性感染及自身免疫性疾病有密切关系。抗生素治疗是HP阳性胃MALT淋巴瘤的一线治疗首选,对于早期病灶局限的MZL患者,以局部治疗为主,放疗或药物治疗之间的选择应“个体化定制”。对于一线治疗无效或晚期全身广泛受累的MZL患者,有治疗指征的患者采用系统性免疫化疗,在一线治疗中应探索高效低毒的无化疗方案。BTK抑制剂、PI3K抑制剂、双特异性抗体和CAR-T细胞等新型免疫、靶向药物在治疗复发难治MZL取得明显疗效,但要实现真正意义上的精准治疗。
边缘区淋巴瘤的规范诊治++第四届中国淋巴瘤个体化治疗大会
【概要描述】MZL概述:流行病学及相关危险因素
边缘区淋巴瘤(MZL)是一组起源于淋巴滤泡的边缘区B细胞淋巴瘤,可发生于脾、淋巴结和黏膜淋巴组织,约占所有非霍奇金淋巴瘤(NHL)的10%。MZL的发病率较低,在西方国家发病率约为5%-15%,在中国的发病率为7.8%。MZL存在较强的异质性,WHO将MZL分为三种类型:结外粘膜相关淋巴组织(MALT)淋巴瘤(EMZL)、脾边缘区B细胞淋巴瘤(SMZL)、淋巴结边缘区淋巴瘤(NMZL),其中MALT淋巴瘤最为常见,约占70%。MZL呈惰性,预后相对较好。EMZL的中位总生存期(OS)>12年,SMZL和NMZL的中位OS>8年。
目前普遍认为MALT淋巴瘤的发生可能与慢性抗原刺激有关,如感染或自身免疫性疾病。幽门螺杆菌、空肠弯曲菌分别与胃、肠MALT淋巴瘤有比较确切的关系。眼附属器MALT淋巴瘤与鹦鹉热衣原体感染相关,皮肤MALT淋巴瘤与疏螺旋体感染存在相关性,HCV感染可致多部位MALT淋巴瘤发生,如脾、唾液腺或泪腺。目前尚未确定肺MALT淋巴瘤的致病原,吸烟与发病关系存在争议。约15%的原发肺MALT淋巴瘤患者合并有自身免疫病,包括多发性硬化、系统性红斑狼疮(SLE)、桥本甲状腺炎、干燥综合征,均为肺MALT淋巴瘤发生的危险因素。
MZL的诊治规范
MZL的病理特征包括肿瘤中包含大量异质性细胞浸润,有中心样细胞、单核细胞、B细胞、小淋巴细胞和浆细胞等,也可能有大细胞和/或幼稚细胞存在。患者生存时间大多数较长,但也有少数病例可呈侵袭性疾病进程。MZL肿瘤细胞表达B细胞相关抗原,如CD19、CD20、CD22、CD79b,MZL患者通常CD10-、CD5-、CD43±、CD3-、CD23-、CD11c±,少数结外患者可见CD5+。MZL亚型的生物机制各不相同,主要通路为NF-κB和NOTCH通路。
对于MZL的病理诊断,双跃荣教授强调了克隆性IG基因重排检测的重要性。部分MALT淋巴瘤可出现t(11;18),预示疾病晚期和抗HP治疗疗效欠佳,需要采用其他治疗方式。对于SMZL,可检测-7q+,3q等染色体异常或NOTCH2、KLF2等基因突变。SMZL可通过检测MYD88突变和淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)鉴别,以及检测BRAF突变与毛细胞白血病进行鉴别。
非胃MALT或NMZL适用Lugano分期,而胃肠MZL则采用AnnArbor分期系统的Lugano改良版或胃肠淋巴瘤的TNM分期(巴黎分期)。SMZL通常为脾单发,通过脾切除进行诊断和分期。
MALT淋巴瘤、SMZL、NMZL拥有各自独立的预后评估系统,相关基因异常可提示预后。MALT淋巴瘤采用IELSG预后模型(MALT-IPI),通过年龄、分期、乳酸脱氢酶(LDH)等危险因素对MALT淋巴瘤患者进行分层。一项基于人群的研究显示:EMZL原发部位和诊断时期对患者的死亡率存在影响。原发部位为泌尿生殖(GU)系统的EMZL患者预后最差,而位于皮肤和结缔组织的患者预后最好。C-myc过表达同样可以预测MALT淋巴瘤的预后不良。一项对62例MALT淋巴瘤患者进行的多因素分析显示,C-myc≥20%具有显著统计学差异。
滤泡性淋巴瘤(FL)的预后指标24月内疾病进展(POD24)在MALT淋巴瘤中同样提示预后不良。IELSG19临床研究显示:接受一线系统性治疗的EMZL患者,出现POD24患者生存率较差,有可能作为未来前瞻性临床研究的终点指标。MALT淋巴瘤出现组织学转化同样提示预后不良。微小残留病(MRD)评估是SMZL的独立预后因素。相关研究显示:骨髓中uMRD(定义为MRD<0.01%)是SMZL患者,尤其是治疗结束后达到部分缓解(PR)的患者的独立预后因素。
双跃荣教授随后对MZL的治疗方式进行了介绍。对于早期病灶局限的MZL患者,治疗以局部治疗为主,包括手术和局部放疗等。对于一线治疗无效局限期患者或晚期全身广泛受累的MZL患者,由于其惰性病程,治疗参考FL,有治疗指征的患者采用系统性免疫化疗。对于复发难治MZL患者可选择来那度胺、BTK抑制剂、PI3K抑制剂、嵌合抗原受体T细胞(CAR-T)等新药治疗。
抗HP治疗是早期胃MALT淋巴瘤的首选治疗方式,相关研究显示:单纯HP治疗可带来长期缓解,完全缓解(CR)率达到80%,71%的患者可获得持续5年的CR,5年总生存(OS)率达到90%。但对于t(11;18)阳性患者,抗HP治疗CR率仅为15%,t(11;18)阳性与治疗无反应及复发显著相关,对于这部分患者需要选择其他治疗方式。局部胃MALT淋巴瘤放射治疗的10年长期随访结果显示:所有患者接受放射治疗后内镜活检均获得CR,5年和10年OS率分别为92%和87%,5年和10年无复发生存(RFS)率分别为88%和77%。目前NCCN指南也推荐放射治疗作为HP阴性和抗生素治疗无效MZL患者的治疗选择。
目前各指南中MALT淋巴瘤的一线治疗方案大多为利妥昔单抗为基础联合放化疗,根据疾病分期和分型选择合适的一线治疗方案。
Stil NHL 7-2008研究探索了BR方案(苯达莫司汀+利妥昔单抗)治疗MZL后利妥昔单抗维持治疗的必要性。研究结果显示:BR治疗后2年利妥昔单抗维持治疗延长了患者的PFS(HR:0.33),但OS无差异。BR方案治疗后利妥昔单抗的维持治疗对于MZL患者是一种可行的治疗方法。
MZL的最新治疗进展
MZL存在众多潜在的治疗靶点,无论是针对MZL一线治疗的R2方案(来那度胺+利妥昔单抗)还是针对复发难治MZL的PI3K/AKT/mTOR抑制剂、BTK抑制剂、CAR-T疗法都值得进行探索。
2020年ASH大会上报道的一项多中心队列研究探索了伊布替尼治疗复发难治MZL的预测因素和结果,研究结果显示:伊布替尼治疗线数不同,PFS或OS无显著差异(2 vs 3 vs 4线及以后);伊布替尼治疗达到CR/PR以及没有复杂细胞遗传学是更好的PFS和OS预测指标。PCYC-1121研究纳入了63例复发难治MZL患者接受伊布替尼治疗。中位随访33.1个月时,伊布替尼治疗复发难治MZL的客观缓解率(ORR)达到58%,缓解持续时间(DOR)为27.6个月,中位PFS为15.7个月,中位OS未达到;在随后14个月中未出现新的不良事件(AE)。该研究同时显示:2项基因突变(A20和MYD88L265P)与预后较好(SPD、PFS)相关;2项基因突变(KMT2D和CARD11)与预后较差(DOR)相关。
2020年ASH大会上同样公布了PI3K抑制剂Parascalisib治疗复发难治MZL的疗效和安全性(CITADEL研究)。研究结果显示:Parascalisib治疗复发难治MZL的ORR达到57%,中位DOR和PFS分别为12个月和19.4个月。
ZUMA-5研究探索了靶向CD19的CAR-T产品axicabtagene ciloleucel(axi-cel)治疗NHL的疗效,研究共纳入22例MZL患者。ZUMA-5研究结果显示:axi-cel治疗MZL的ORR达到85%,CR率为60%,中位DOR为10.6个月;MZL组患者的中位PFS为11.8个月,12个月PFS率为45.1%,中位OS未达到,12个月OS率为92.9%。
总结
双跃荣教授最后总结道:MZL是来源于B细胞的惰性淋巴瘤,其病因与多种微生物慢性感染及自身免疫性疾病有密切关系。抗生素治疗是HP阳性胃MALT淋巴瘤的一线治疗首选,对于早期病灶局限的MZL患者,以局部治疗为主,放疗或药物治疗之间的选择应“个体化定制”。对于一线治疗无效或晚期全身广泛受累的MZL患者,有治疗指征的患者采用系统性免疫化疗,在一线治疗中应探索高效低毒的无化疗方案。BTK抑制剂、PI3K抑制剂、双特异性抗体和CAR-T细胞等新型免疫、靶向药物在治疗复发难治MZL取得明显疗效,但要实现真正意义上的精准治疗。
- 分类:其他血液病
- 作者:编辑
- 来源:互联网
- 发布时间:2021-03-25 14:33
- 访问量:
MZL概述:流行病学及相关危险因素
边缘区淋巴瘤(MZL)是一组起源于淋巴滤泡的边缘区B细胞淋巴瘤,可发生于脾、淋巴结和黏膜淋巴组织,约占所有非霍奇金淋巴瘤(NHL)的10%。MZL的发病率较低,在西方国家发病率约为5%-15%,在中国的发病率为7.8%。MZL存在较强的异质性,WHO将MZL分为三种类型:结外粘膜相关淋巴组织(MALT)淋巴瘤(EMZL)、脾边缘区B细胞淋巴瘤(SMZL)、淋巴结边缘区淋巴瘤(NMZL),其中MALT淋巴瘤最为常见,约占70%。MZL呈惰性,预后相对较好。EMZL的中位总生存期(OS)>12年,SMZL和NMZL的中位OS>8年。
目前普遍认为MALT淋巴瘤的发生可能与慢性抗原刺激有关,如感染或自身免疫性疾病。幽门螺杆菌、空肠弯曲菌分别与胃、肠MALT淋巴瘤有比较确切的关系。眼附属器MALT淋巴瘤与鹦鹉热衣原体感染相关,皮肤MALT淋巴瘤与疏螺旋体感染存在相关性,HCV感染可致多部位MALT淋巴瘤发生,如脾、唾液腺或泪腺。目前尚未确定肺MALT淋巴瘤的致病原,吸烟与发病关系存在争议。约15%的原发肺MALT淋巴瘤患者合并有自身免疫病,包括多发性硬化、系统性红斑狼疮(SLE)、桥本甲状腺炎、干燥综合征,均为肺MALT淋巴瘤发生的危险因素。
MZL的诊治规范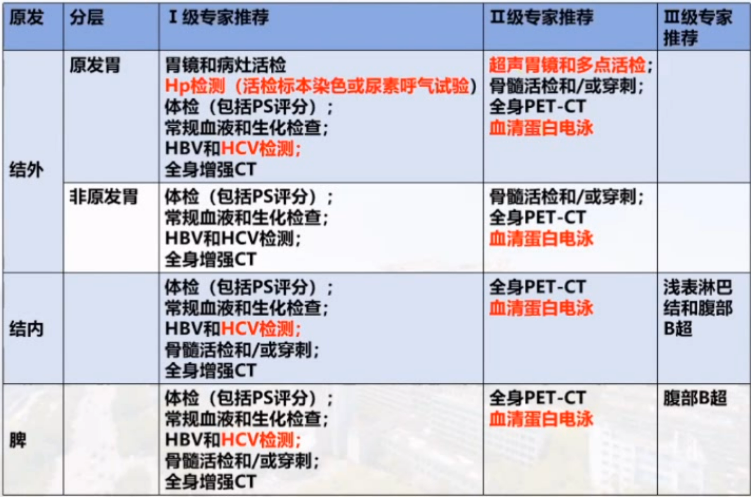
MZL的病理特征包括肿瘤中包含大量异质性细胞浸润,有中心样细胞、单核细胞、B细胞、小淋巴细胞和浆细胞等,也可能有大细胞和/或幼稚细胞存在。患者生存时间大多数较长,但也有少数病例可呈侵袭性疾病进程。MZL肿瘤细胞表达B细胞相关抗原,如CD19、CD20、CD22、CD79b,MZL患者通常CD10-、CD5-、CD43±、CD3-、CD23-、CD11c±,少数结外患者可见CD5+。MZL亚型的生物机制各不相同,主要通路为NF-κB和NOTCH通路。
对于MZL的病理诊断,双跃荣教授强调了克隆性IG基因重排检测的重要性。部分MALT淋巴瘤可出现t(11;18),预示疾病晚期和抗HP治疗疗效欠佳,需要采用其他治疗方式。对于SMZL,可检测-7q+,3q等染色体异常或NOTCH2、KLF2等基因突变。SMZL可通过检测MYD88突变和淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)鉴别,以及检测BRAF突变与毛细胞白血病进行鉴别。
非胃MALT或NMZL适用Lugano分期,而胃肠MZL则采用AnnArbor分期系统的Lugano改良版或胃肠淋巴瘤的TNM分期(巴黎分期)。SMZL通常为脾单发,通过脾切除进行诊断和分期。

MALT淋巴瘤、SMZL、NMZL拥有各自独立的预后评估系统,相关基因异常可提示预后。MALT淋巴瘤采用IELSG预后模型(MALT-IPI),通过年龄、分期、乳酸脱氢酶(LDH)等危险因素对MALT淋巴瘤患者进行分层。一项基于人群的研究显示:EMZL原发部位和诊断时期对患者的死亡率存在影响。原发部位为泌尿生殖(GU)系统的EMZL患者预后最差,而位于皮肤和结缔组织的患者预后最好。C-myc过表达同样可以预测MALT淋巴瘤的预后不良。一项对62例MALT淋巴瘤患者进行的多因素分析显示,C-myc≥20%具有显著统计学差异。
滤泡性淋巴瘤(FL)的预后指标24月内疾病进展(POD24)在MALT淋巴瘤中同样提示预后不良。IELSG19临床研究显示:接受一线系统性治疗的EMZL患者,出现POD24患者生存率较差,有可能作为未来前瞻性临床研究的终点指标。MALT淋巴瘤出现组织学转化同样提示预后不良。微小残留病(MRD)评估是SMZL的独立预后因素。相关研究显示:骨髓中uMRD(定义为MRD<0.01%)是SMZL患者,尤其是治疗结束后达到部分缓解(PR)的患者的独立预后因素。
双跃荣教授随后对MZL的治疗方式进行了介绍。对于早期病灶局限的MZL患者,治疗以局部治疗为主,包括手术和局部放疗等。对于一线治疗无效局限期患者或晚期全身广泛受累的MZL患者,由于其惰性病程,治疗参考FL,有治疗指征的患者采用系统性免疫化疗。对于复发难治MZL患者可选择来那度胺、BTK抑制剂、PI3K抑制剂、嵌合抗原受体T细胞(CAR-T)等新药治疗。
抗HP治疗是早期胃MALT淋巴瘤的首选治疗方式,相关研究显示:单纯HP治疗可带来长期缓解,完全缓解(CR)率达到80%,71%的患者可获得持续5年的CR,5年总生存(OS)率达到90%。但对于t(11;18)阳性患者,抗HP治疗CR率仅为15%,t(11;18)阳性与治疗无反应及复发显著相关,对于这部分患者需要选择其他治疗方式。局部胃MALT淋巴瘤放射治疗的10年长期随访结果显示:所有患者接受放射治疗后内镜活检均获得CR,5年和10年OS率分别为92%和87%,5年和10年无复发生存(RFS)率分别为88%和77%。目前NCCN指南也推荐放射治疗作为HP阴性和抗生素治疗无效MZL患者的治疗选择。
目前各指南中MALT淋巴瘤的一线治疗方案大多为利妥昔单抗为基础联合放化疗,根据疾病分期和分型选择合适的一线治疗方案。

Stil NHL 7-2008研究探索了BR方案(苯达莫司汀+利妥昔单抗)治疗MZL后利妥昔单抗维持治疗的必要性。研究结果显示:BR治疗后2年利妥昔单抗维持治疗延长了患者的PFS(HR:0.33),但OS无差异。BR方案治疗后利妥昔单抗的维持治疗对于MZL患者是一种可行的治疗方法。
MZL的最新治疗进展
MZL存在众多潜在的治疗靶点,无论是针对MZL一线治疗的R2方案(来那度胺+利妥昔单抗)还是针对复发难治MZL的PI3K/AKT/mTOR抑制剂、BTK抑制剂、CAR-T疗法都值得进行探索。
2020年ASH大会上报道的一项多中心队列研究探索了伊布替尼治疗复发难治MZL的预测因素和结果,研究结果显示:伊布替尼治疗线数不同,PFS或OS无显著差异(2 vs 3 vs 4线及以后);伊布替尼治疗达到CR/PR以及没有复杂细胞遗传学是更好的PFS和OS预测指标。PCYC-1121研究纳入了63例复发难治MZL患者接受伊布替尼治疗。中位随访33.1个月时,伊布替尼治疗复发难治MZL的客观缓解率(ORR)达到58%,缓解持续时间(DOR)为27.6个月,中位PFS为15.7个月,中位OS未达到;在随后14个月中未出现新的不良事件(AE)。该研究同时显示:2项基因突变(A20和MYD88L265P)与预后较好(SPD、PFS)相关;2项基因突变(KMT2D和CARD11)与预后较差(DOR)相关。
2020年ASH大会上同样公布了PI3K抑制剂Parascalisib治疗复发难治MZL的疗效和安全性(CITADEL研究)。研究结果显示:Parascalisib治疗复发难治MZL的ORR达到57%,中位DOR和PFS分别为12个月和19.4个月。
ZUMA-5研究探索了靶向CD19的CAR-T产品axicabtagene ciloleucel(axi-cel)治疗NHL的疗效,研究共纳入22例MZL患者。ZUMA-5研究结果显示:axi-cel治疗MZL的ORR达到85%,CR率为60%,中位DOR为10.6个月;MZL组患者的中位PFS为11.8个月,12个月PFS率为45.1%,中位OS未达到,12个月OS率为92.9%。
总结
双跃荣教授最后总结道:MZL是来源于B细胞的惰性淋巴瘤,其病因与多种微生物慢性感染及自身免疫性疾病有密切关系。抗生素治疗是HP阳性胃MALT淋巴瘤的一线治疗首选,对于早期病灶局限的MZL患者,以局部治疗为主,放疗或药物治疗之间的选择应“个体化定制”。对于一线治疗无效或晚期全身广泛受累的MZL患者,有治疗指征的患者采用系统性免疫化疗,在一线治疗中应探索高效低毒的无化疗方案。BTK抑制剂、PI3K抑制剂、双特异性抗体和CAR-T细胞等新型免疫、靶向药物在治疗复发难治MZL取得明显疗效,但要实现真正意义上的精准治疗。
相关信息

服务号

订阅号
无极血康中医医院 冀ICP备05003291号-1 网站建设:中企动力 石家庄 SEO



