自体血液/骨髓移植后患者的远期死亡和预期寿命的变化趋势
- 分类:医学进展
- 作者:血康医院
- 来源:互联网
- 发布时间:2022-03-31 10:50
- 访问量:
【概要描述】自体血液/骨髓移植(blood or marrow transplantation,BMT)是目前公认的许多血液肿瘤的治疗方法。尽管支持治疗方案的改进使患者早期死亡率显著下降,但自体BMT受者由于远期疾病负担,他们的远期死亡风险仍然较高。远期死亡的主要原因包括疾病的复发或进展以及继发性恶性肿瘤(SMN)。但是,研究者尚不清楚远期发病率和死亡率对预期寿命的累积影响。 在过去30年间,移植方案变化很大,具体包括:移植时患者年龄增大;因浆细胞病(PCD)选择自体BMT的患者增多;全身照射(TBI)作为移植前治疗的减少;选择外周血干细胞(PBSC)作为干细胞来源的增多。然而,研究者尚不明确这些因素对死亡率和预期寿命的影响。基于此,有研究者开展了BMT生存者研究,探究了BMT治疗后生存≥2年的患者远期死亡和预期寿命的变化趋势。 研究方法 BMT生存者研究(BMT Survivor Study)是希望之城国家医疗中心、明尼苏达大学和阿拉巴马大学伯明翰分校三个医疗中心合作的研究项目。该研究纳入了2014年及之前于三个医疗中心接受BMT治疗后生存≥2年的患者。研究人群的主要暴露变量为接受BMT治疗的四个不同时期:1981-1999年;2000-2005年;2006-2010年;2011-2014年。随访截止日期为2021年4月19日。 研究结果 患者基线特征 该研究共纳入了4702例患者,接受BMT时的中位年龄为53岁(范围:0-78岁),58.7%患者为男性,67.8%为非西班牙裔白种人,28.3%患者于2011-2014年间接受了BMT治疗。BMT治疗后中位随访时间为9年(范围:2-36年)。PCD是接受BMT治疗的最常见病因(42.3%)。91.6%患者移植时选择PBSC作为干细胞来源,23.1%接受TBI作为移植前治疗。按四个时期分层(1981-1999;2000-2005;2006-2010;2011-2014),BMT时的中位年龄从40岁增至58岁,PCD患者的比例从13.7%增至60.0%,以PBSC作为干细胞来源的患者比例从66.6%增至99.5%;而接受TBI作为移植前治疗的患者从56.4%降至5.2%,以及因急性髓系白血病(AML)/骨髓增生异常综合征(MDS)接受BMT患者比例从15.4%降至0.2%。具体基线特征如表1。 表1 死亡率与预期寿命 BMT后2-30年的死亡率高于预期,曲线呈U型,随访时间最短的患者与最长的患者间差异较大;BMT后2年死亡率为39.2/1000人/年,BMT后30年死亡率为54.1/1000人/年。各年龄移植患者的死亡率均高于预期;>30岁移植的患者与普通人群相比,死亡率差异越来越大。该研究队列的全因死亡风险是普通人群的2.1倍(95%CI,2.0-2.2)。具体如图1。 图1 以BMT后存活≥2年为前提条件,患者预期寿命减少7.0年,即减少了25.8%。越年轻的患者寿命减少年数越多,老年患者减少最少。具体如图2。 图2 按四个时期分层,2011-2014的预期寿命减少为9.4%,1981-1999年预期寿命减少为18.5%。校正相关人口统计学和临床变量后,全因死亡率的5年风险比以1981-1999为参考,其余三个时期均有所下降。具体如图3。 图3 四个时期的未校正5年全因死亡率风险比具有可比性。校正BMT时年龄和初步诊断,均降低了死亡率风险比。对BMT时年龄、初步诊断和TBI三个因素校正后,从1981-1999至2011-2014的晚期死亡率进一步降低。根据BMT时年龄进行分层分析(≤40岁;41-64岁;≥65岁)的结果,≥65岁患者四个时期的远期全因死亡率显著下降;根据早期诊断的分层分析结果,PCD和霍奇金淋巴瘤患者四个时期的远期全因死亡率显著下降;根据TBI进行分层分析结果,未接受TBI治疗的患者四个时期的远期全因死亡率显著下降。 远期死亡风险 以BMT后头2年存活为前提条件,整个研究队列的25年总生存率为41.0%。与远期全因死亡相关的因素包括BMT时年龄较大(41-64岁:HR=2.47,95%CI,2.14-2.86;≥65岁:HR=3.69,95%CI,3.08-4.42;参考年龄组:0-40岁)、男性(HR=1.17,95%CI,1.07-1.28)和高危疾病(HR=1.34;95%CI,1.20-1.50)。具体如表2。 表2 在2132例死亡患者中,1898例(89.0%)可知晓死因。死亡原因包复发相关死亡(RRM,47.4%)、非复发死亡(NRM,44.0%)和外部原因(1.6%)。25年RRM累积发生率为23.8%(95%CI,22.5-25.2),NRM为25.9%(95%CI,24.0-27.7)。NRM最常见原因包括感染(n=361)、SMN(n=346)、心血管疾病(n=260)和肾脏疾病(n=165)。感染相关死亡的25年累积发生率为9.7%,标准死亡比(SMR)为8.1。多变量分析表明接受BMT时年龄较大、高危疾病和PCD是感染相关死亡率的预测因素。SMN相关死亡的25年累积发生率为9.8%,SMR为5.7。SMN的类型包括血液系统SMN(治疗相关髓系肿瘤[t-MN:n=124]和其他[n=23])和实体SMN(胃肠道肿瘤[n=56]、肺部肿瘤[n=47]和其他[n=93])。多变量分析表明BMT时年龄较大是所有SMN、t-MN和实体SMN相关死亡率的预测因素,而男性是实体SMN相关死亡率的预测因素。 近年间BMT受者的死亡率和预期寿命 该研究整理了2006-2014年间接受BMT治疗的2546例患者的数据结果。以存活≥2年为前提条件,该亚组患者全因死亡率风险比普通人群高9.1倍(95%CI,8.51-9.69),15年总生存率为53.4%。15年RRM累积发生率为22.3%,NRM为17.4%。与RRM相关的因素包括BMT时年龄较大、高危疾病和PCD。与NRM相关的因素包括BMT时年龄较大、男性、亚洲人种、高危疾病、移植前TBI治疗以及使用骨髓作为干细胞来源。与正常人群相比,该组别患者的预期寿命缩短了4.4年。 研究结论 该研究结果表明,BMT受者的远期死亡率在30年间有所下降。但是,还需要进一步控制感染、继发性肿瘤、心血管和肾脏疾病的发生发展,进而降低远期死亡率。 参考文献: Smita Bhatia, Chen Dai, Wendy Landier, et al. Trends in Late Mortality and Life Expectancy After Autologous Blood or Marrow Transplantation Over Three Decades: A BMTSS Report. J Clin Oncol. 2022 Mar 9;JCO2102372. doi: 10.1200/JCO.21.02372.
自体血液/骨髓移植后患者的远期死亡和预期寿命的变化趋势
【概要描述】自体血液/骨髓移植(blood or marrow transplantation,BMT)是目前公认的许多血液肿瘤的治疗方法。尽管支持治疗方案的改进使患者早期死亡率显著下降,但自体BMT受者由于远期疾病负担,他们的远期死亡风险仍然较高。远期死亡的主要原因包括疾病的复发或进展以及继发性恶性肿瘤(SMN)。但是,研究者尚不清楚远期发病率和死亡率对预期寿命的累积影响。
在过去30年间,移植方案变化很大,具体包括:移植时患者年龄增大;因浆细胞病(PCD)选择自体BMT的患者增多;全身照射(TBI)作为移植前治疗的减少;选择外周血干细胞(PBSC)作为干细胞来源的增多。然而,研究者尚不明确这些因素对死亡率和预期寿命的影响。基于此,有研究者开展了BMT生存者研究,探究了BMT治疗后生存≥2年的患者远期死亡和预期寿命的变化趋势。
研究方法
BMT生存者研究(BMT Survivor Study)是希望之城国家医疗中心、明尼苏达大学和阿拉巴马大学伯明翰分校三个医疗中心合作的研究项目。该研究纳入了2014年及之前于三个医疗中心接受BMT治疗后生存≥2年的患者。研究人群的主要暴露变量为接受BMT治疗的四个不同时期:1981-1999年;2000-2005年;2006-2010年;2011-2014年。随访截止日期为2021年4月19日。
研究结果
患者基线特征
该研究共纳入了4702例患者,接受BMT时的中位年龄为53岁(范围:0-78岁),58.7%患者为男性,67.8%为非西班牙裔白种人,28.3%患者于2011-2014年间接受了BMT治疗。BMT治疗后中位随访时间为9年(范围:2-36年)。PCD是接受BMT治疗的最常见病因(42.3%)。91.6%患者移植时选择PBSC作为干细胞来源,23.1%接受TBI作为移植前治疗。按四个时期分层(1981-1999;2000-2005;2006-2010;2011-2014),BMT时的中位年龄从40岁增至58岁,PCD患者的比例从13.7%增至60.0%,以PBSC作为干细胞来源的患者比例从66.6%增至99.5%;而接受TBI作为移植前治疗的患者从56.4%降至5.2%,以及因急性髓系白血病(AML)/骨髓增生异常综合征(MDS)接受BMT患者比例从15.4%降至0.2%。具体基线特征如表1。
表1
死亡率与预期寿命
BMT后2-30年的死亡率高于预期,曲线呈U型,随访时间最短的患者与最长的患者间差异较大;BMT后2年死亡率为39.2/1000人/年,BMT后30年死亡率为54.1/1000人/年。各年龄移植患者的死亡率均高于预期;>30岁移植的患者与普通人群相比,死亡率差异越来越大。该研究队列的全因死亡风险是普通人群的2.1倍(95%CI,2.0-2.2)。具体如图1。
图1
以BMT后存活≥2年为前提条件,患者预期寿命减少7.0年,即减少了25.8%。越年轻的患者寿命减少年数越多,老年患者减少最少。具体如图2。
图2
按四个时期分层,2011-2014的预期寿命减少为9.4%,1981-1999年预期寿命减少为18.5%。校正相关人口统计学和临床变量后,全因死亡率的5年风险比以1981-1999为参考,其余三个时期均有所下降。具体如图3。
图3
四个时期的未校正5年全因死亡率风险比具有可比性。校正BMT时年龄和初步诊断,均降低了死亡率风险比。对BMT时年龄、初步诊断和TBI三个因素校正后,从1981-1999至2011-2014的晚期死亡率进一步降低。根据BMT时年龄进行分层分析(≤40岁;41-64岁;≥65岁)的结果,≥65岁患者四个时期的远期全因死亡率显著下降;根据早期诊断的分层分析结果,PCD和霍奇金淋巴瘤患者四个时期的远期全因死亡率显著下降;根据TBI进行分层分析结果,未接受TBI治疗的患者四个时期的远期全因死亡率显著下降。
远期死亡风险
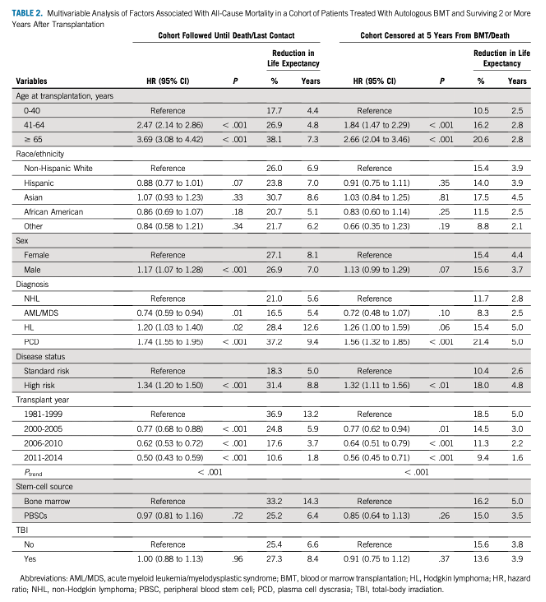
以BMT后头2年存活为前提条件,整个研究队列的25年总生存率为41.0%。与远期全因死亡相关的因素包括BMT时年龄较大(41-64岁:HR=2.47,95%CI,2.14-2.86;≥65岁:HR=3.69,95%CI,3.08-4.42;参考年龄组:0-40岁)、男性(HR=1.17,95%CI,1.07-1.28)和高危疾病(HR=1.34;95%CI,1.20-1.50)。具体如表2。
表2
在2132例死亡患者中,1898例(89.0%)可知晓死因。死亡原因包复发相关死亡(RRM,47.4%)、非复发死亡(NRM,44.0%)和外部原因(1.6%)。25年RRM累积发生率为23.8%(95%CI,22.5-25.2),NRM为25.9%(95%CI,24.0-27.7)。NRM最常见原因包括感染(n=361)、SMN(n=346)、心血管疾病(n=260)和肾脏疾病(n=165)。感染相关死亡的25年累积发生率为9.7%,标准死亡比(SMR)为8.1。多变量分析表明接受BMT时年龄较大、高危疾病和PCD是感染相关死亡率的预测因素。SMN相关死亡的25年累积发生率为9.8%,SMR为5.7。SMN的类型包括血液系统SMN(治疗相关髓系肿瘤[t-MN:n=124]和其他[n=23])和实体SMN(胃肠道肿瘤[n=56]、肺部肿瘤[n=47]和其他[n=93])。多变量分析表明BMT时年龄较大是所有SMN、t-MN和实体SMN相关死亡率的预测因素,而男性是实体SMN相关死亡率的预测因素。
近年间BMT受者的死亡率和预期寿命
该研究整理了2006-2014年间接受BMT治疗的2546例患者的数据结果。以存活≥2年为前提条件,该亚组患者全因死亡率风险比普通人群高9.1倍(95%CI,8.51-9.69),15年总生存率为53.4%。15年RRM累积发生率为22.3%,NRM为17.4%。与RRM相关的因素包括BMT时年龄较大、高危疾病和PCD。与NRM相关的因素包括BMT时年龄较大、男性、亚洲人种、高危疾病、移植前TBI治疗以及使用骨髓作为干细胞来源。与正常人群相比,该组别患者的预期寿命缩短了4.4年。
研究结论
该研究结果表明,BMT受者的远期死亡率在30年间有所下降。但是,还需要进一步控制感染、继发性肿瘤、心血管和肾脏疾病的发生发展,进而降低远期死亡率。
参考文献:
Smita Bhatia, Chen Dai, Wendy Landier, et al. Trends in Late Mortality and Life Expectancy After Autologous Blood or Marrow Transplantation Over Three Decades: A BMTSS Report. J Clin Oncol. 2022 Mar 9;JCO2102372. doi: 10.1200/JCO.21.02372.
- 分类:医学进展
- 作者:血康医院
- 来源:互联网
- 发布时间:2022-03-31 10:50
- 访问量:
自体血液/骨髓移植(blood or marrow transplantation,BMT)是目前公认的许多血液肿瘤的治疗方法。尽管支持治疗方案的改进使患者早期死亡率显著下降,但自体BMT受者由于远期疾病负担,他们的远期死亡风险仍然较高。远期死亡的主要原因包括疾病的复发或进展以及继发性恶性肿瘤(SMN)。但是,研究者尚不清楚远期发病率和死亡率对预期寿命的累积影响。
在过去30年间,移植方案变化很大,具体包括:移植时患者年龄增大;因浆细胞病(PCD)选择自体BMT的患者增多;全身照射(TBI)作为移植前治疗的减少;选择外周血干细胞(PBSC)作为干细胞来源的增多。然而,研究者尚不明确这些因素对死亡率和预期寿命的影响。基于此,有研究者开展了BMT生存者研究,探究了BMT治疗后生存≥2年的患者远期死亡和预期寿命的变化趋势。
研究方法
BMT生存者研究(BMT Survivor Study)是希望之城国家医疗中心、明尼苏达大学和阿拉巴马大学伯明翰分校三个医疗中心合作的研究项目。该研究纳入了2014年及之前于三个医疗中心接受BMT治疗后生存≥2年的患者。研究人群的主要暴露变量为接受BMT治疗的四个不同时期:1981-1999年;2000-2005年;2006-2010年;2011-2014年。随访截止日期为2021年4月19日。
研究结果
患者基线特征
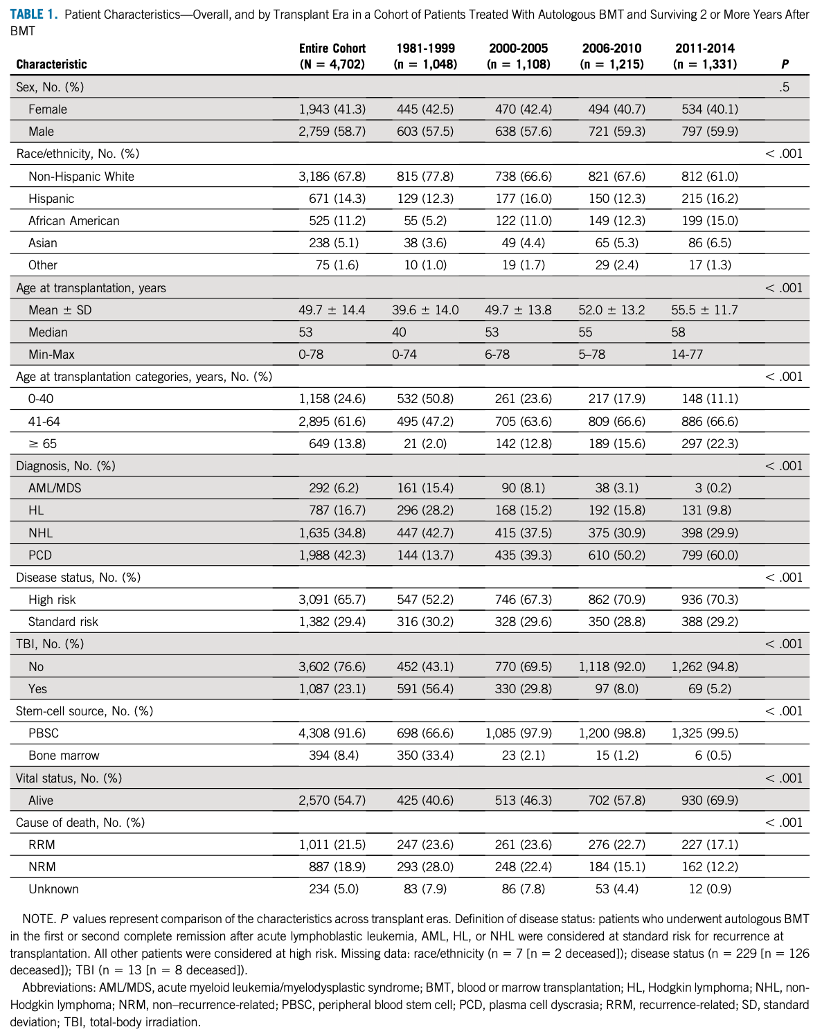
该研究共纳入了4702例患者,接受BMT时的中位年龄为53岁(范围:0-78岁),58.7%患者为男性,67.8%为非西班牙裔白种人,28.3%患者于2011-2014年间接受了BMT治疗。BMT治疗后中位随访时间为9年(范围:2-36年)。PCD是接受BMT治疗的最常见病因(42.3%)。91.6%患者移植时选择PBSC作为干细胞来源,23.1%接受TBI作为移植前治疗。按四个时期分层(1981-1999;2000-2005;2006-2010;2011-2014),BMT时的中位年龄从40岁增至58岁,PCD患者的比例从13.7%增至60.0%,以PBSC作为干细胞来源的患者比例从66.6%增至99.5%;而接受TBI作为移植前治疗的患者从56.4%降至5.2%,以及因急性髓系白血病(AML)/骨髓增生异常综合征(MDS)接受BMT患者比例从15.4%降至0.2%。具体基线特征如表1。
表1
死亡率与预期寿命
BMT后2-30年的死亡率高于预期,曲线呈U型,随访时间最短的患者与最长的患者间差异较大;BMT后2年死亡率为39.2/1000人/年,BMT后30年死亡率为54.1/1000人/年。各年龄移植患者的死亡率均高于预期;>30岁移植的患者与普通人群相比,死亡率差异越来越大。该研究队列的全因死亡风险是普通人群的2.1倍(95%CI,2.0-2.2)。具体如图1。
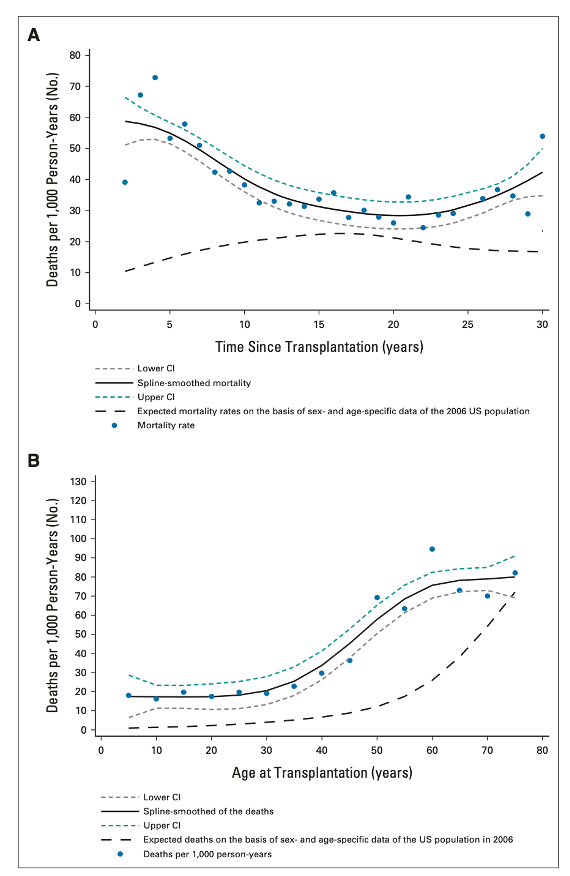
图1
以BMT后存活≥2年为前提条件,患者预期寿命减少7.0年,即减少了25.8%。越年轻的患者寿命减少年数越多,老年患者减少最少。具体如图2。
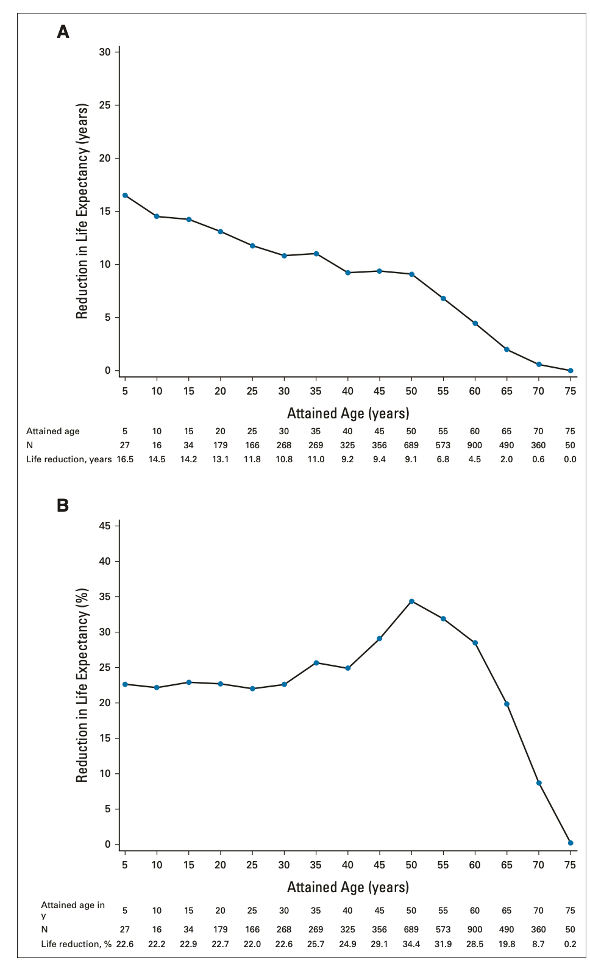
图2
按四个时期分层,2011-2014的预期寿命减少为9.4%,1981-1999年预期寿命减少为18.5%。校正相关人口统计学和临床变量后,全因死亡率的5年风险比以1981-1999为参考,其余三个时期均有所下降。具体如图3。
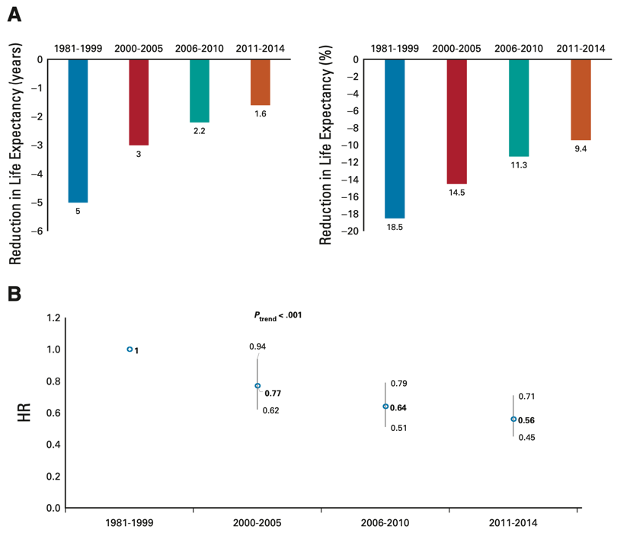
图3
四个时期的未校正5年全因死亡率风险比具有可比性。校正BMT时年龄和初步诊断,均降低了死亡率风险比。对BMT时年龄、初步诊断和TBI三个因素校正后,从1981-1999至2011-2014的晚期死亡率进一步降低。根据BMT时年龄进行分层分析(≤40岁;41-64岁;≥65岁)的结果,≥65岁患者四个时期的远期全因死亡率显著下降;根据早期诊断的分层分析结果,PCD和霍奇金淋巴瘤患者四个时期的远期全因死亡率显著下降;根据TBI进行分层分析结果,未接受TBI治疗的患者四个时期的远期全因死亡率显著下降。
远期死亡风险
以BMT后头2年存活为前提条件,整个研究队列的25年总生存率为41.0%。与远期全因死亡相关的因素包括BMT时年龄较大(41-64岁:HR=2.47,95%CI,2.14-2.86;≥65岁:HR=3.69,95%CI,3.08-4.42;参考年龄组:0-40岁)、男性(HR=1.17,95%CI,1.07-1.28)和高危疾病(HR=1.34;95%CI,1.20-1.50)。具体如表2。
表2
在2132例死亡患者中,1898例(89.0%)可知晓死因。死亡原因包复发相关死亡(RRM,47.4%)、非复发死亡(NRM,44.0%)和外部原因(1.6%)。25年RRM累积发生率为23.8%(95%CI,22.5-25.2),NRM为25.9%(95%CI,24.0-27.7)。NRM最常见原因包括感染(n=361)、SMN(n=346)、心血管疾病(n=260)和肾脏疾病(n=165)。感染相关死亡的25年累积发生率为9.7%,标准死亡比(SMR)为8.1。多变量分析表明接受BMT时年龄较大、高危疾病和PCD是感染相关死亡率的预测因素。SMN相关死亡的25年累积发生率为9.8%,SMR为5.7。SMN的类型包括血液系统SMN(治疗相关髓系肿瘤[t-MN:n=124]和其他[n=23])和实体SMN(胃肠道肿瘤[n=56]、肺部肿瘤[n=47]和其他[n=93])。多变量分析表明BMT时年龄较大是所有SMN、t-MN和实体SMN相关死亡率的预测因素,而男性是实体SMN相关死亡率的预测因素。
近年间BMT受者的死亡率和预期寿命
该研究整理了2006-2014年间接受BMT治疗的2546例患者的数据结果。以存活≥2年为前提条件,该亚组患者全因死亡率风险比普通人群高9.1倍(95%CI,8.51-9.69),15年总生存率为53.4%。15年RRM累积发生率为22.3%,NRM为17.4%。与RRM相关的因素包括BMT时年龄较大、高危疾病和PCD。与NRM相关的因素包括BMT时年龄较大、男性、亚洲人种、高危疾病、移植前TBI治疗以及使用骨髓作为干细胞来源。与正常人群相比,该组别患者的预期寿命缩短了4.4年。
研究结论
该研究结果表明,BMT受者的远期死亡率在30年间有所下降。但是,还需要进一步控制感染、继发性肿瘤、心血管和肾脏疾病的发生发展,进而降低远期死亡率。
参考文献:
Smita Bhatia, Chen Dai, Wendy Landier, et al. Trends in Late Mortality and Life Expectancy After Autologous Blood or Marrow Transplantation Over Three Decades: A BMTSS Report. J Clin Oncol. 2022 Mar 9;JCO2102372. doi: 10.1200/JCO.21.02372.
相关信息

服务号

订阅号
无极血康中医医院 冀ICP备05003291号-1 网站建设:中企动力 石家庄 SEO



